
Diketahui unsur 9 F , 17 Cl , 35 Br dan 53 I . Urutkan da...
Cara pengukuran jari-jari atom logam dan non logam ditunjukkan seperti pada gambar. Gambar. Jari-jari Al dan Cl 2.. Pada tabel dapat kamu lihat bahwa keelektronegatifan fluor memiliki harga keelektronegatifan terbesar yaitu 4, artinya fluor paling mudah menarik elektron dari atom lain. Fransium dengan harga keelektronegatifan paling rendah.

Pembahasan soal Sifat Keperiodikan Unsur (Keelektronegatifan terbesar dan terkecil) YouTube
Dengan demikian, elektron-elektron akan tertarik mendekati klorida dan menjauhi natrium. 3. Gunakan tabel elektronegativitas sebagai referensi. Tabel elektronegativitas unsur memiliki unsur yang disusun tepat seperti dalam tabel periodik, kecuali bahwa setiap atom dilabeli dengan elektronegativitasnya masing-masing.
Data Keelektronegatifan Beberapa Unsur Sebagai Berikut Unsur Yang Paling Elektropositif Adalah
Elektronegativitas atau keelektronegatifan (Simbol: χ) adalah sebuah sifat kimia yang menjelaskan kemampuan sebuah atom (atau lebih jarangnya sebuah gugus fungsi) untuk menarik elektron (atau rapatan elektron) menuju dirinya sendiri pada ikatan kovalen. Konsep elektronegativitas pertama kali oleh Linus Pauling pada tahun 1932 sebagai bagian dari perkembangan teori ikatan valensi.

Keelektronegatifan / Elektronegatifitas Suatu Unsur Adalah Sifat Yang Menyatakan tujuan dari
Keelektronegatifan adalah kemampuan suatu atom untuk menarik elektron ke dalam ikatannya ketika atomatom tersebut membentuk ikatan. Keelektronegatifan diukur dengan menggunakan skala Pauling yang besarnya antara 0,7 sampai 4. Yang mana, unsur yang mempunyai harga keelektronegatifan besar, cenderung menerima elektron dan akan membentuk ion negatif.

Unsur Yang Mempunyai Keelektronegatifan Terbesar Adalah Berbagai Unsur
Jadi keelektronegatifan terbesar berada pada golongan VIIA. 1. Membuat konfigurasi elektron masing-masing unsur. 2. Menentukan unsur yang paling elektronegatif. Semakin ke atas dan semakin ke kanan (golongan VIIA) letak suatu unsur dalam tabel periodik maka keelektronegatifan semakin besar.

Data Keelektronegatifan Beberapa Unsur Sebagai Berikut Unsur Yang Paling Elektropositif Adalah
Cara Mudah Menjawab Soal Energi Ionisasi Pemahaman mengenai energi ionisasi dan penjelasan mengenai cara mudah menentukan urutan unsur dan kestabilan unsur b.
Cara Menentukan Periode Dan Golongan Unsur Dari Konfigurasi Elektron My XXX Hot Girl
Ilustrasi Interaksi Atom Dengan Nilai Keelektronegatifan Rendah dan Tinggi Saat Berikatan, Gambar Oleh I.N.G Wardana. Nah, begitulah kira-kira bagaimana cara Linus Pauling berfikir pada saat akan menentukan rumus besar atau kecilnya nilai keelektronegatifan atom pada tabel periodik.

Jelaskan Energi Ionisasi dan Keelektronegatifan? Fisika Kimia
Adapun, unsur dengan keelektronegatifan terbesar adalah fluor dan unsur yang paling rendah keelektronegatifitasnnya adalah fransium. Baca juga: Sifat Periodik Unsur. Jenis ikatan kimia yang dihasilkan. Keelektronegatifan dua atom akan menentukan jenis ikatan kimia yang dihasilkan.
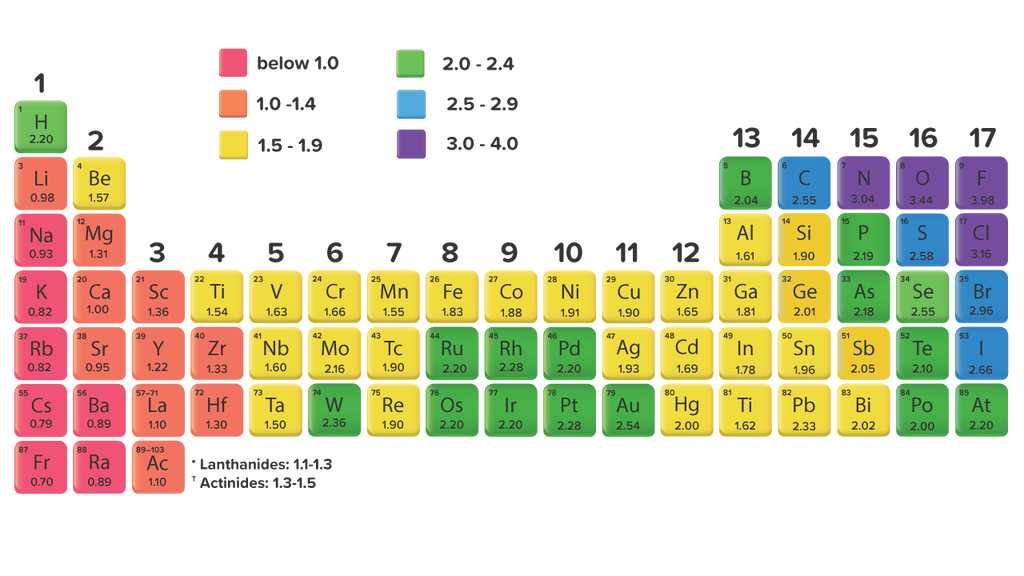
Unsur yang memiliki keeletronegatifan paling tingg...
Sedangkan, keelektronegatifan adalah kemampuan atom menarik elektron. Artinya, energi ionisasi dan keelektronegatifan adalah kebalikan. Dilansir dari Thought Co, atom dengan energi ionisasi yang rendah memiliki keelektronegatifan yang rendah juga karena inti atomnya tidak memberikan gaya tarik menarik yang kuat terhadap elektron.

Rangkuman Dan Latihan Soal Konfigurasi Elektron Periode Dan Golongan My XXX Hot Girl
Sama halnya dengan jari-jari atom, sifat keperiodikan unsur yang satu ini juga memiliki kecenderungan sebagai berikut: Dalam satu golongan dari atas ke bawah, energi ionisasi suatu unsur semakin kecil dikarenakan jari-jari atom bertambah besar, sehingga daya tarik inti terhadap elektron terluar semakin lemah dan energi ionisasi berkurang.

Cara Mudah Menjawab Soal Keelektronegatifan (Kimia SBMPTN, UN, SMA) YouTube
Pembahasan Soal #3: Senyawa yang atom-atamnya memiliki perbedaan keelektronegatifan terbesar bersifat lebih ionik, sebaliknya yang memiliki perbedaan keelektronegatifan terkecil ia akan dominan karakter kovalennya. ∆ keelektronegatifan AB → |4,0 - 3,3| = 0,7. ∆ keelektronegatifan AD → |4,0 - 1,3| = 2,7.
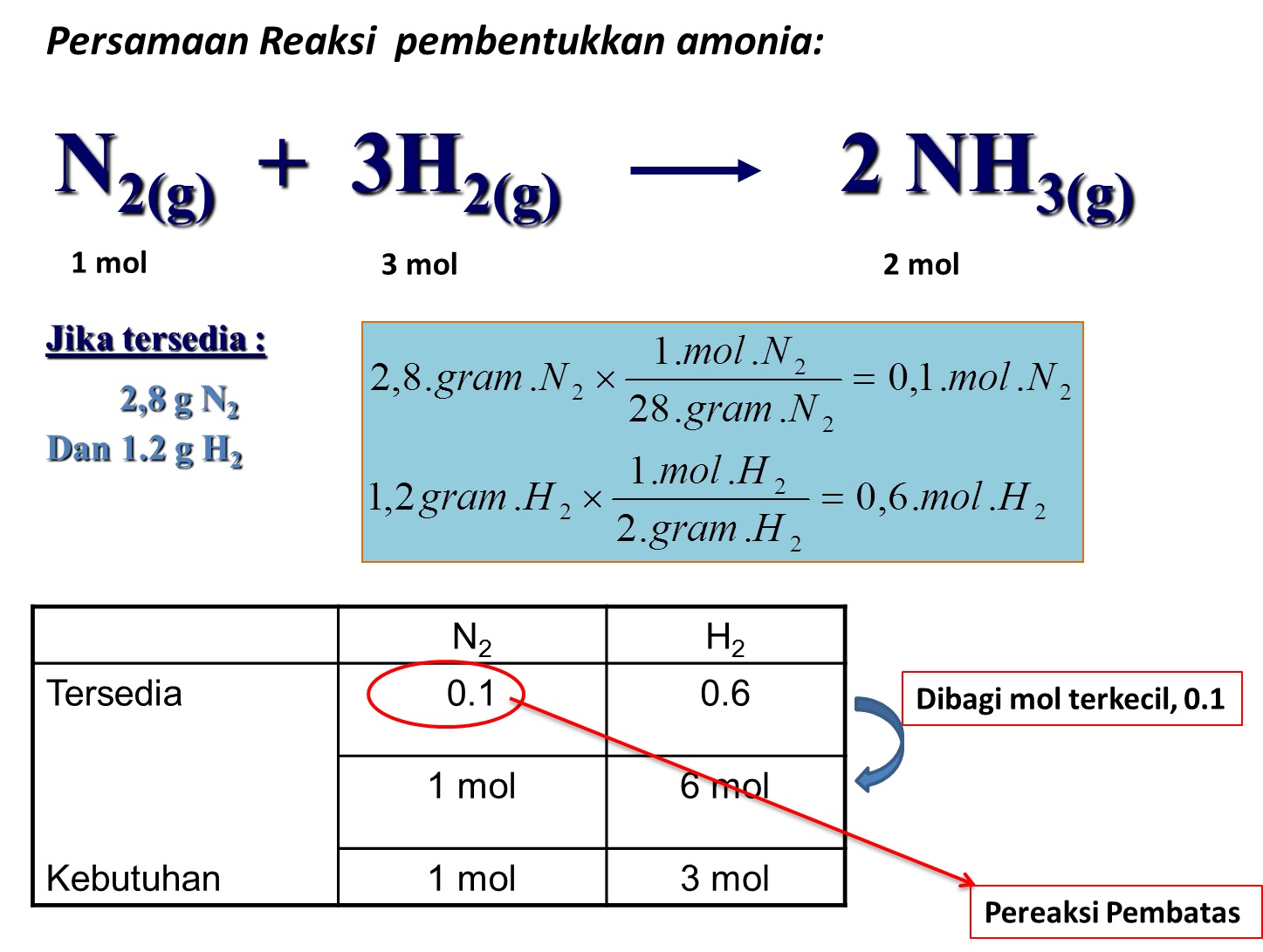
Cara Menentukan Pereaksi Pembatas Dalam Reaksi Kimia My XXX Hot Girl
Cara Menghitung Energi Ionisasi Cara menentukan energi ionisasi dapat dilakukan menggunakan Model Atom Bohr. Model tersebut akan memprediksi beberapa jalur bagi elektron pada saat mengelilingi inti yang mengandung proton dan neutron. Rumus energi ionisasi dengan model Bohr dapat dituliskan sebagai berikut: En = - 2π² Me⁴/4πϵ₀ Z²/N²

Keelektronegatifan Terbesar YouTube
Oleh karena itu tidak ada sifat tertentu yang dapat diukur untuk menentukan atau membandingkan kelektronegatifan unsur-unsur. Tabel Skala Pauli (Tabel Keelektronegatifan Unsur) Linus Carl Pauling (1901-1994) membuat sebuah skala nilai Keelektronegatifan yang terkenal dengan sebutan skala Pauling .

Suatu Unsur X Dengan Nomor Atom Mempunyai Jumlah Orbital Seputar Nomor My XXX Hot Girl
Skala Pauling merupakan skala yang digunakan untuk menentukan nilai keelektronegatifan pada tabel periodik. 3. Bagaimana cara menghitung keelektronegatifan? Untuk menghitung keelektronegatifan, kamu dapat menggunakan tabel periodik atau rumus: keelektronegatifan = 0,5 x (nilai elektronegativitas unsur A + nilai elektronegativitas unsur B). 4.

Keelektronegatifan Ujian
Cara mudah menentukan urutan jari jari atom, keelektronegatifan, energi ionisasi dan Afinitas elektron di Sistem Periodik Unsur.Jika menemui soal seperti ini.

latihan soal UN keelektronegatifan dalam Satu golongan kimia SMA YouTube
Avogadro dan ahli kimia lain mengkaji keelektronegatifan sebelum ia dinamakan secara rasmi oleh Jöns Jacob Berzelius pada tahun 1811. Pada tahun 1932, Linus Pauling mencadangkan skala keelektronegatifan berdasarkan tenaga ikatan . Nilai keelektronegatifan pada skala Pauling ialah nombor tanpa dimensi yang berjalan dari kira-kira 0.7 hingga 3.98.